创伤、感染、肿瘤、先天性畸形、骨质疏松等因素可引起不同程度的骨缺损。尽管骨缺损具有自愈能力,但超过临界尺寸的骨缺损无法自愈。近年来,骨组织工程(bone tissue engineering, BTE)被认为是最有前途的骨修复与重建方法,并取得了巨大成功。支架材料、种子细胞和生长因子被称为BTE的三要素。然而,支架的物理性质和生物相容性以及生长因子的安全性和成本,限制了它们在临床上的应用。因此,开发一种用高效生长因子修饰的新型支架以满足 BTE 的要求至关重要。

图为:文章首页
基于此,博辉瑞进联合天津医科大学第二医院、天津医科大学口腔医学院、天津市中诺口腔医院专家团队,开发了用新型融合肽修饰的三维打印聚乳酸-乙醇酸共聚物/羟基磷灰石(PLGA/HA)复合支架,它能有效促进骨缺损的再生和修复。
在本项研究中,研究人员制备了具有适当HA含量的3D打印PLGA/HA复合支架,并使其具有适当的力学性能。此外,用新的融合肽修饰了3D打印的聚乳酸(PLGA)/羟基磷灰石(HA)复合支架的表面,使其具有成骨、抗菌和促进血管生成的作用。
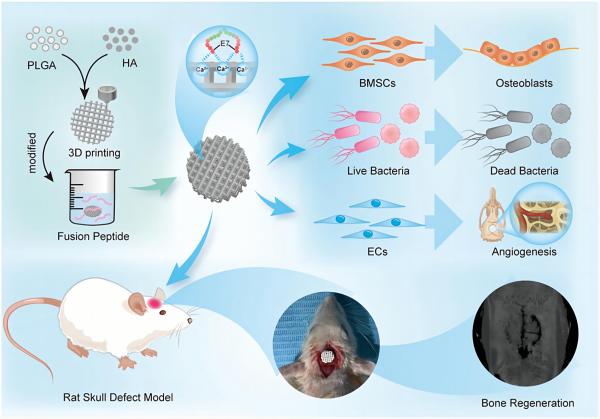
图为:3D-PLGA/HA功能化支架的制备及大鼠颅骨缺损修复示意图
体外实验表明,融合肽修饰的支架具有良好的生物相容性和一定的抗菌活性。此外,融合肽改性支架还能显著提高骨髓间充质干细胞(BMSCs)和Ea.hy926细胞的迁移能力,促进BMSCs成骨相关因子(BMP2、RUNX2、ALP、OPN)的表达,促进Ea.hy926细胞血管生成相关因子(VEGF和HIF-1α)的表达。
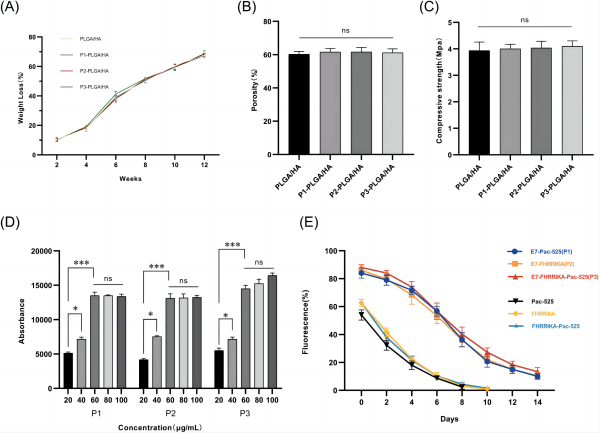
图为:样品的表征。(A) PLGA/HA支架的降解率。(B) PLGA/HA支架的孔隙率。(C) PLGA/HA支架抗压强度。(D)不同浓度融合肽溶液孵育3d后的荧光强度。(E)不同肽溶液孵育不同时间后支架上的残留荧光强度

图为:样品对骨髓间充质干细胞增殖、迁移及成骨分化的影响。(A) CCK-8实验显示骨髓间充质干细胞和Ea的增殖。各组培养1、3、5、7 d后的hy926细胞。(B) BMSCs和Ea.hy926细胞的AO染色图像。(C) Transwell实验评估BMSCs和Ea.hy926细胞在样品表面培养的迁移能力
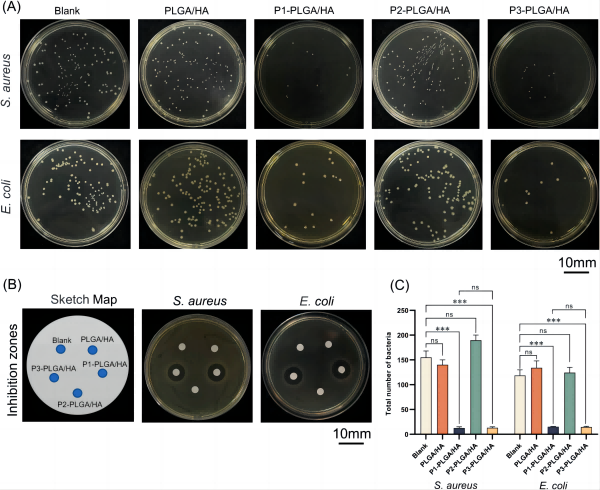
图为:样品的体外抗菌活性。(A, C)总抑菌活性检测及菌落定量分析。(B)与样品提取物共培养24 h细菌的抑制区(误差条代表n=3时的平均值±SD)
体内实验表明,负载融合肽的支架材料具有更好的骨传导性和骨诱导性,骨缺损部位的骨组织再生量明显大于空白对照组。空白支架材料由于不含功能因子,具有一定的骨传导性,但不具有骨诱导能力,因此融合肽修饰的3D-PLGA/HA支架更有利于修复关键骨缺损部位。
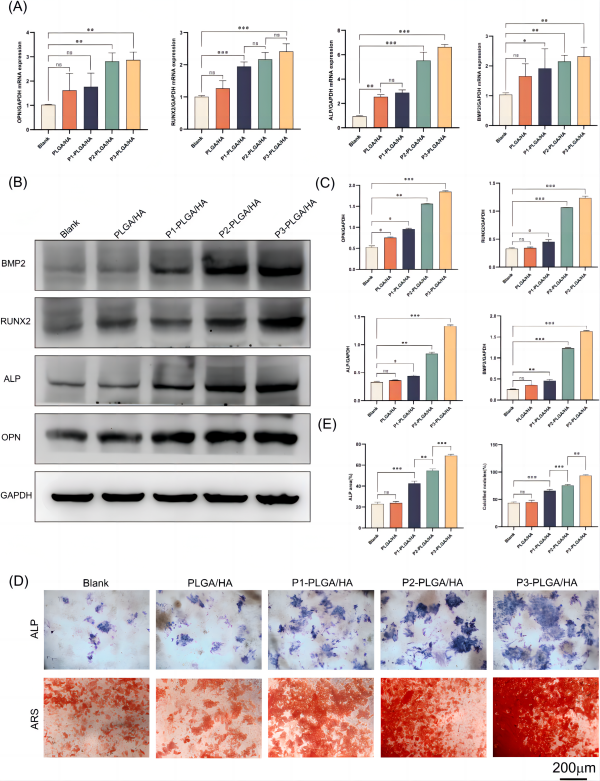
图为:样品对骨髓间充质干细胞成骨因子表达的影响。(A)成骨相关基因的Real-time PCR分析。(B)成骨相关蛋白的Western blot分析。(C) Western blot数据的定量分析。(D)骨髓间充质干细胞的ALP (7 D)和ARS染色(21 D)图像。(E) ALP和ARS染色定量分析
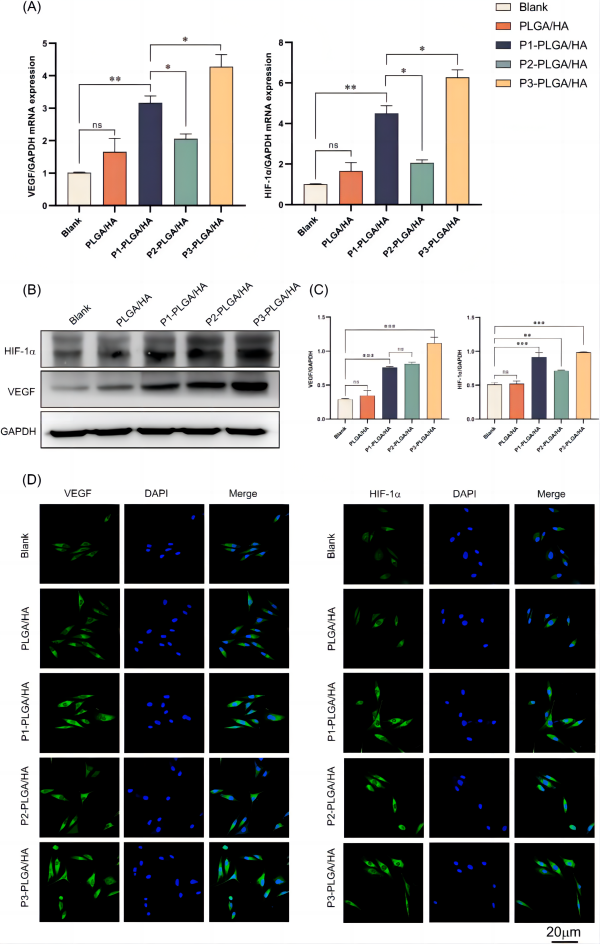
图为:样品对Ea.hy926细胞血管生成相关因子表达的影响(A)血管生成相关基因的实时PCR分析。(B)血管生成相关蛋白的Western blot分析。(C) Western blot数据的定量分析。(D) Ea.hy926细胞血管生成相关蛋白(血管生成相关蛋白:绿色,细胞核:蓝色)的免疫荧光分析
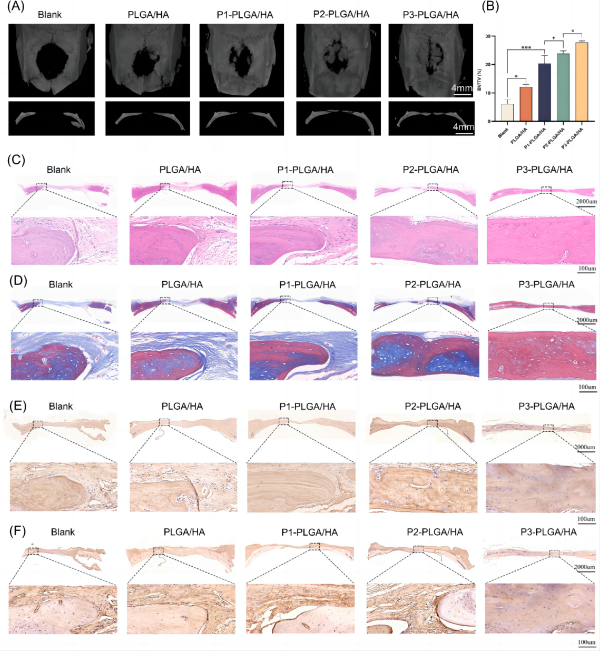
图为:3 m处颅骨缺损模型成骨能力评估。(A)不同样品覆盖骨缺损的三维重建和矢状面图像。(B)不同组骨缺损BV/TV。(C) H&E染色。(D)Masson三色染色。(E) OCN表达的免疫组织化学分析。(F) Col-I表达的免疫组织化学分析
总结:研究人员成功制备了具有合适HA组分含量和机械强度的3D打印PLGA/HA复合支架材料,并实现了融合肽对PLGA/HA支架的多功能修饰。P3-PLGA/HA复合支架具有良好的生物活性和安全性,可促进BMSCs和Ea.hy926细胞的迁移。P3-PLGA/HA复合支架还能促进骨髓间充质干细胞中OPN、RUNX2、ALP、BMP2的表达以及Ea.hy926细胞中VEGF、HIF-α的表达,显著抑制金黄色葡萄球菌和大肠杆菌的生长,形成骨缺损部位具有良好成骨潜能的骨传导和骨诱导复合支架材料。本研究为BTE在骨缺损修复中的应用提供了更好的选择。
近日,该研究成果已获材料科学领域国际期刊《Journal of Materials Research and Technology》收录,文章标题《A 3D-printed PLGA/HA composite scaffold modified with fusion peptides to enhance its antibacterial, osteogenic and angiogenic properties in bone defect repair》,影响因子6.4。
博辉瑞进自主研发、具有自主知识产权的骨填充修复材料技术平台,采用脱细胞外基质凝胶与羟基磷灰石复合,具有骨引导的同时,提高了骨填充材料的生物相容性。SIS凝胶中含有生物活性因子,可促进血管再生,进一步促进骨修复,SIS凝胶的相关研究已经发表多篇SCI论文(Cell Proliferation ,2022,Volume55.,Journal of Materials Chemistry B,2022, 10, 6279-6286.,ACS Applied Materials & Interfaces,2022, 14, 38525-38540.)。同时,羟基磷灰石颗粒表面具有多孔结构,促进细胞长入,有助于新骨的生成,羟基磷灰石的相关研究也已经发表在Advanced Functional Materials, 2024: 2315382.,ACS Applied Materials & Interfaces, 2024.业界权威期刊上。博辉瑞进骨填充修复材料在口腔颌面外科、神经外科及四肢脊柱外科均有潜在的应用前景,相关产品正在注册取证过程中。

2024年12月6日,为期三天的SDHE...

理智弄槽外科韵,巴山蜀水天府情。2024...

6月11日,由中华口腔医学会主办的“口腔...

近日,《中华胸心血管外科杂志》2024年...

2024年5月9日,在VBEF未来医疗生...

新春伊始,万象更新。博辉瑞进迎来新春“开...

12月22日,《陕西省际联盟硬脑(脊)膜...

落叶飘零随风拂,初冬悄然而至。随着冬天一...

清风入梦时,春和正景明。四月芳菲至,等你...

对一个家庭来说,最大的喜事之一,莫过于添...
版权所有北京博辉瑞进生物科技有限公司 京ICP备16026579号 (京)-非经营性-2017-0030  京公网安备 11011502006176号 (京)网药械信息备字(2022)第00096号
京公网安备 11011502006176号 (京)网药械信息备字(2022)第00096号