马年启新程,捷报踏春来。
马年开工伊始,博辉瑞进传来重磅捷报:公司核心产品硬脑(脊)膜修补片正式获批香港医疗器械行政管理制度(MDACS)IV类注册证书,成功纳入香港特别行政区政府卫生署医疗器械表列清单。这一突破,不仅标志着博辉瑞进在高端植入生物医用材料领域的技术实力、产品质量与全流程合规体系获得高标准认可,为公司打开香港市场提供了准入基础,同时也为公司进一步拓展更为广阔的海外市场、深化全球化战略布局奠定了坚实根基。

作为博辉瑞进自主创新研发的SIS生物材料平台的核心产品之一,硬脑(脊)膜修补片于2021年取得国家药品监督管理局III类医疗器械注册证获批上市,已在临床实现广泛应用,为患者提供安全可靠的治疗保障。该产品可应用于多种神经外科手术场景,能有效降低脑脊液渗漏并发症的发生风险;力学强度适宜,适配临床精细化操作需求;材料本身富含天然生物活性因子,可内源性诱导组织再生,且能随新生组织生长完成同步吸收、完全降解;同时具备优异的抗感染性能,是临床理想的硬脑(脊)膜修复替代材料。
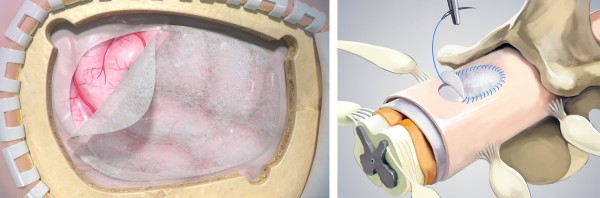
香港作为亚洲医疗创新枢纽及国际医疗技术交流的重要窗口,其MDACS注册体系具有严苛的审核标准。其中,IV类医疗器械作为最高风险等级品类,需通过安全性、有效性的全面验证,以及质量管理体系的严格核查,是对产品技术成熟度与临床可靠性的全面检验。博辉瑞进硬脑(脊)膜修补片顺利获批,不仅印证了产品在复杂手术场景中保障患者安全、实现精准修复的核心价值,更彰显了博辉瑞进在高端植入生物医用材料领域的自主创新实力。
此次香港市场准入,是博辉瑞进全球化布局的又一重要里程碑。截至目前,博辉瑞进多款产品已相继获批中国NMPA、欧盟CE、美国FDA、越南MOH等多个国家和地区的权威认证,初步构建起覆盖全球主要市场的销售体系。依托香港MDACS表列资质,博辉瑞进将具备进入香港大型公立医院采购体系资格,为当地患者带来高品质的国产植入医疗器械产品。未来,博辉瑞进将积极建立与香港医疗机构、高校及科研平台的产学研医合作,加速推进硬脑(脊)膜修补片在香港市场的临床落地,同时以香港为窗口,为公司拓展海外医疗合作、深化国际市场影响力奠定坚实基础,为全球患者提供更优质的产品解决方案,持续践行“以患者为中心,以先进的再生医学材料技术,为卓越外科提供全面解决方案”的企业使命。

《中国肺癌杂志》2024年6月第27卷第...

2024年12月6日,为期三天的SDHE...

理智弄槽外科韵,巴山蜀水天府情。2024...

近日,《中华胸心血管外科杂志》2024年...

2024年5月9日,在VBEF未来医疗生...

新春伊始,万象更新。博辉瑞进迎来新春“开...
版权所有北京博辉瑞进生物科技股份有限公司 京ICP备16026579号 (京)-非经营性-2017-0030  京公网安备 11011502006176号 药品医疗器械网络信息服务备案(京)网药械信息备字(2022)第00096号
京公网安备 11011502006176号 药品医疗器械网络信息服务备案(京)网药械信息备字(2022)第00096号